| Etilene | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| etene | |
| Nomi alternativi | |
| etilene gas di olefina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H4 |
| Massa molecolare (u) | 28,054 |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 200-815-3 |
| PubChem | 6325 |
| SMILES | C=C |
| Proprietà chimico-fisiche | |
| Densità (kg·m−3, in c.s.) | 1,2612 |
| Solubilità in acqua | 131 mg/L (25 °C) |
| Temperatura di fusione | −169,2 °C (104 K) |
| ΔfusH0 (kJ·mol−1) | 3,35 |
| ΔfusS0 (J·K−1mol−1) | 32,2 |
| Temperatura di ebollizione | −103,7 °C (169,4 K) |
| ΔebH0 (kJ·mol−1) | 13,544 |
| ΔebS0 (J·K−1mol−1) | 79,95 |
| Punto triplo | -169 °C (104,0 K) 120 Pa |
| Punto critico | 9,35 °C (282,5 K) 5,06 × 106 Pa |
| Tensione di vapore (Pa) a 273 K | 4,1 × 106 |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | 52,4 |
| ΔfG0 (kJ·mol−1) | 68,4 |
| S0m(J·K−1mol−1) | 219,3 |
| C0p,m(J·K−1mol−1) | 42,9 |
| Indicazioni di sicurezza | |
| Punto di fiamma | −136 °C (137 K) |
| Limiti di esplosione | 2,7 – 36% |
| Temperatura di autoignizione | 450 °C (723 K) |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 220 - 280 - 336 |
| Consigli P | 210 - 260 - 304+340 - 315 - 377 - 381 - 405 - 403 [1] |
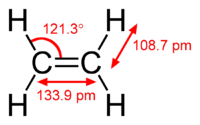
L'etilene (nome IUPAC: etene) è il più semplice degli alcheni, avente formula chimica C2H4. A temperatura e pressione ambiente si presenta come un gas incolore, estremamente infiammabile,dal lieve odore dolce, muschiato e un po' pungente.[2] Oltre ad essere un importante prodotto nell'industria chimica (è ad esempio il composto chimico da cui si ottiene il polietilene), è anche un ormone (per la maturazione) di molte specie vegetali (fitormone).[3] È un anestetico e come tale fu usato fino a circa il 1940.[4]
Il gruppo funzionale corrispondente a una molecola di etilene privata di un atomo di idrogeno, il più semplice degli alchenili, si chiama comunemente vinile e i composti contenenti tale gruppo sono detti composti vinilici.
- ^ scheda dell'etilene su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ (EN) Heinz Zimmermann e Roland Walzl, Ethylene, Wiley-VCH Verlag GmbH & Co. KGaA, 15 aprile 2009, pp. a10_045.pub3, DOI:10.1002/14356007.a10_045.pub3, ISBN 978-3-527-30673-2. URL consultato il 31 dicembre 2021.
- ^ (EN) Kevin L.-C. Wang, Hai Li e Joseph R. Ecker, Ethylene Biosynthesis and Signaling Networks, in The Plant Cell, vol. 14, suppl 1, 2002-05, pp. S131–S151, DOI:10.1105/tpc.001768. URL consultato il 31 dicembre 2021.
- ^ (EN) Francis X. Whalen, Douglas R. Bacon e Hugh M. Smith, Inhaled anesthetics: an historical overview, in Best Practice & Research Clinical Anaesthesiology, vol. 19, n. 3, 2005-09, pp. 323–330, DOI:10.1016/j.bpa.2005.02.001. URL consultato il 31 dicembre 2021.